2020-2026年中國仿制藥市場評估與發(fā)展前景報告
http://www.diannaozhi.com 2020-07-17 09:24 中企顧問網(wǎng)
2020-2026年中國仿制藥市場評估與發(fā)展前景報告2020-7
中國制藥市場規(guī)模由2013年的1618億美元增至2017年的2118億美元,預(yù)計2022年將增至3305億美元,該期間的復(fù)合年增長率為9.3%。增長主要受人口老齡化及慢性病患病率相應(yīng)上升以及中國政府的優(yōu)惠政策推動,該政策旨在開發(fā)中國高質(zhì)量創(chuàng)新藥物及生物制劑市場,增加可支配收入及擴大承保范圍。
中國制藥市場規(guī)模對比
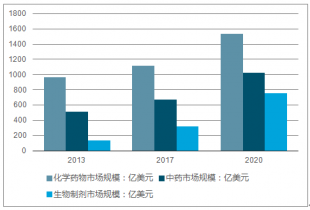
中國仿制藥和專利藥市場規(guī)模對比
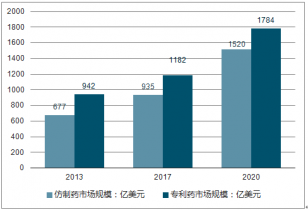
中企顧問網(wǎng)發(fā)布的《2020-2026年中國仿制藥市場評估與發(fā)展前景報告》共四章。首先介紹了中國仿制藥行業(yè)市場發(fā)展環(huán)境、仿制藥整體運行態(tài)勢等,接著分析了中國仿制藥行業(yè)市場運行的現(xiàn)狀,然后介紹了仿制藥市場競爭格局。隨后,報告對仿制藥做了重點企業(yè)經(jīng)營狀況分析,最后分析了中國仿制藥行業(yè)發(fā)展趨勢與投資預(yù)測。您若想對仿制藥產(chǎn)業(yè)有個系統(tǒng)的了解或者想投資中國仿制藥行業(yè),本報告是您不可或缺的重要工具。
本研究報告數(shù)據(jù)主要采用國家統(tǒng)計數(shù)據(jù),海關(guān)總署,問卷調(diào)查數(shù)據(jù),商務(wù)部采集數(shù)據(jù)等數(shù)據(jù)庫。其中宏觀經(jīng)濟數(shù)據(jù)主要來自國家統(tǒng)計局,部分行業(yè)統(tǒng)計數(shù)據(jù)主要來自國家統(tǒng)計局及市場調(diào)研數(shù)據(jù),企業(yè)數(shù)據(jù)主要來自于國統(tǒng)計局規(guī)模企業(yè)統(tǒng)計數(shù)據(jù)庫及證券交易所等,價格數(shù)據(jù)主要來自于各類市場監(jiān)測數(shù)據(jù)庫。
報告目錄:
1.1仿制藥綜述
1.1.1仿制藥的概念分析
1.1.2仿制藥的特征分析
1.2國外仿制藥發(fā)展狀況分析
1.2.1美國仿制藥發(fā)展分析
(1)美國仿制藥市場發(fā)展狀況分析
(2)美國仿制藥發(fā)展歷程
(3)美國仿制藥發(fā)展現(xiàn)狀
(4)美國仿制藥發(fā)展經(jīng)驗借鑒
1.2.2日本仿制藥發(fā)展分析
(1)日本仿制藥市場發(fā)展狀況分析
(2)日本仿制藥發(fā)展歷程
(3)日本仿制藥發(fā)展現(xiàn)狀
(4)日本仿制藥發(fā)展經(jīng)驗借鑒
1.3國內(nèi)仿制藥發(fā)展狀況分析
1.3.1中國仿制藥市場發(fā)展規(guī)模分析
中國仿制藥市場規(guī)模走勢
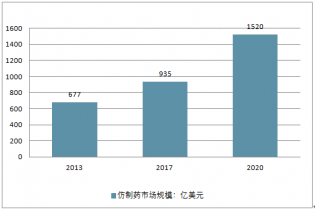
1.3.2仿制藥相關(guān)政策分析
(1)國家層面政策環(huán)境分析
1)行業(yè)相關(guān)標準
2)行業(yè)相關(guān)政策
3)行業(yè)發(fā)展規(guī)劃
(2)地方層面政策環(huán)境分析
1)青海省仿制藥政策分析
2)廣東省仿制藥政策分析
3)四川省仿制藥政策分析
4)安徽省仿制藥政策分析
5)其他省市仿制藥政策分析
1.3.3仿制藥發(fā)展歷程分析
1.3.4仿制藥發(fā)展現(xiàn)狀分析
1.3.5仿制藥發(fā)展痛點分析
(1)確定參比制劑困難大
(2)企業(yè)藥學研究難度大
(3)臨床試驗資源嚴重短缺
第2章:仿制藥對醫(yī)藥行業(yè)的影響分析
2.1仿制藥對藥物制劑行業(yè)的影響分析
2.1.1中國藥物制劑行業(yè)發(fā)展現(xiàn)狀
(1)藥物制劑行業(yè)市場規(guī)模分析
(2)藥物制劑行業(yè)競爭格局分析
2.1.2仿制藥對行業(yè)的影響分析
(1)國內(nèi)企業(yè)強者恒強,合縱連橫
(2)出口企業(yè)迎來國內(nèi)拓展機會
2.1.3藥物制劑行業(yè)發(fā)展前景與趨勢
2.2仿制藥對藥用輔料行業(yè)的影響分析
2.2.1中國藥用輔料行業(yè)發(fā)展現(xiàn)狀
(1)藥用輔料行業(yè)市場規(guī)模分析
(2)藥用輔料行業(yè)競爭格局分析
2.2.2仿制藥對行業(yè)的影響分析
2.2.3藥用輔料行業(yè)發(fā)展前景與趨勢
2.3仿制藥對CRO行業(yè)的影響分析
2.3.1中國CRO行業(yè)發(fā)展現(xiàn)狀
(1)CRO行業(yè)市場規(guī)模分析
(2)CRO行業(yè)競爭格局分析
2.3.2仿制藥對行業(yè)的影響分析
2.3.3CRO行業(yè)發(fā)展前景與趨勢
第3章:中國領(lǐng)先醫(yī)藥企業(yè)仿制藥發(fā)展分析
3.1醫(yī)藥企業(yè)仿制藥發(fā)展概況
3.2領(lǐng)先醫(yī)藥企業(yè)仿制藥發(fā)展分析
3.2.1杭州泰格醫(yī)藥科技股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.2浙江華海藥業(yè)股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.3深圳市海王生物工程股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.4安徽山河藥用輔料股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.5浙江京新藥業(yè)股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.6深圳信立泰藥業(yè)股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.7江蘇恒瑞醫(yī)藥股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.8華潤雙鶴藥業(yè)股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.9浙江海正藥業(yè)股份有限公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
3.2.10人福醫(yī)藥集團股份公司
(1)企業(yè)發(fā)展簡況分析
(2)企業(yè)技術(shù)資質(zhì)能力分析
(3)企業(yè)仿制藥發(fā)展分析
(4)企業(yè)市場渠道與網(wǎng)絡(luò)分析
(5)企業(yè)經(jīng)營情況分析
第4章:中國仿制藥市場預(yù)測與投資規(guī)劃
4.1仿制藥發(fā)展前景與趨勢預(yù)測
4.1.1市場發(fā)展環(huán)境分析
4.1.2市場發(fā)展前景預(yù)測
4.1.3市場發(fā)展趨勢預(yù)測
4.2仿制藥市場投資現(xiàn)狀分析
4.2.1市場投資主體分析
(1)市場投資主體構(gòu)成
(2)各投資主體投資優(yōu)勢
4.2.2市場投資切入方式及操作策略
4.2.3市場投資規(guī)模分析
4.2.4市場投資動向分析
4.3仿制藥市場投資策略規(guī)劃
4.3.1投資方式策略規(guī)劃
4.3.2投資區(qū)域策略規(guī)劃
4.3.3投資領(lǐng)域策略規(guī)劃
4.3.4商業(yè)模式策略規(guī)劃
圖表目錄:
圖表1:關(guān)鍵名詞解釋
圖表2:流程中部分重要環(huán)節(jié)
圖表3:全球各國各國仿制藥在總處方量中的使用數(shù)量占比
圖表4:FDA仿制藥科學監(jiān)管發(fā)展歷程
圖表5:美國發(fā)展歷史
圖表6:美國仿制藥前后仿制藥市場發(fā)展對比
圖表7:美國橙皮書中認定參比藥品的基本原則
圖表8:我國當前“仿制藥”現(xiàn)狀與美國1938-1962年仿制藥行業(yè)相似
圖表9:中國與美國仿制藥監(jiān)管方面的區(qū)別
圖表10:日本仿制藥市場份額占比
圖表11:日本仿制藥發(fā)展歷程
圖表12:中國仿制藥相關(guān)標準匯總
圖表13:中國仿制藥行業(yè)相關(guān)政策分析
圖表14:仿制藥流程及關(guān)鍵步驟
圖表15:工作時間表模擬(24-30個月)
圖表16:2018年底完成仿制藥的產(chǎn)品及企業(yè)數(shù)
圖表17:仿制藥涉及批文最多的15個藥品
圖表18:參比制劑選擇原則及確定方式
圖表19:藥學研究或成為相當部分企業(yè)不可逾越的障礙
圖表20:藥物臨床試驗面臨四大約束
圖表21:BE臨床試驗機構(gòu)承接情況
圖表22:涉及到醫(yī)藥產(chǎn)業(yè)鏈當中大部分環(huán)節(jié)
圖表23:帶來巨大的品種“整合”機會
圖表24:企業(yè)選擇的主要考量因素
圖表25:中國部分通過國際化制劑認證的藥企名單
圖表26:帶來輔料企業(yè)格局重整
圖表27:2007-2015年(前)中國CRO市場規(guī)模及增速(單位:億元,%)
圖表28:目前我國CRO市場呈現(xiàn)金字塔型分布
圖表29:不同CRO公司在臨床研究中的主要業(yè)務(wù)布局
圖表30:2018年前必須完成基藥口服藥產(chǎn)品數(shù)TOP20企業(yè)








